
Το συγκεκριμένο άρθρο είναι μια συνέχεια του άρθρου, Τέσσερις (4) διυλιστηριακοί τύποι πυρκαγιών, 16 Οκτωβρίου 2013, Fire.gr.
Τα παρακάτω αέρια που παρουσιάζουμε είναι τα πιο επικίνδυνα αέρια που συναντάμε συχνότερα σε περιβάλλον διυλιστηρίων και πετροχημικών εγκαταστάσεων. Η παρουσίαση τους έχει σκοπό την ενημέρωση του ευρέως πυροσβεστικού προσωπικού που θα κριθεί να αντιμετωπίσει περιστατικά σε τέτοιου είδους περιβάλλον.
Αιθάνιο (ethane, C2H6 )
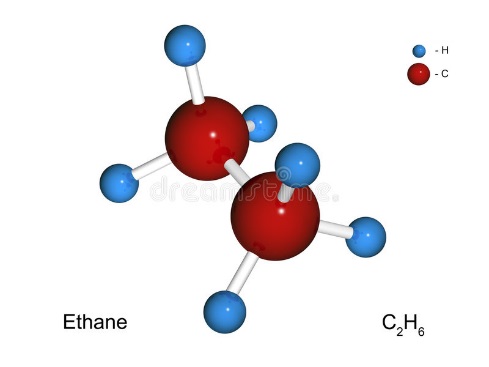
Είναι οργανική χημική ένωση, που περιέχει άνθρακα και υδρογόνο, με μοριακό τύπο C2H6 Είναι άχρωμο και άοσμο, με κρίσιμη θερμοκρασία 32,2°C και κρίσιμη πίεση 48,36 atm. Εξαιρετικά εύφλεκτο αέριο. Σε βιομηχανική κλίμακα το αιθάνιο απομονώνεται από το φυσικό αέριο και από το αργό πετρέλαιο, ως ένα παραπροϊόν της διύλισής του. Από διαρροή αερίου σχηματίζονται με τον αέρα εκρηκτικά μείγματα σε θερμοκρασία περιβάλλοντος. Υπάρχει κίνδυνος φωτιάς από μηχανική κρούση, τριβή, σπινθήρες, φλόγες ή άλλες πήγες ανάφλεξης. Έχει μεγάλο εύρος συγκεντρώσεων από 2% – 10% κατ’ όγκο οπού σχηματίζει εκρηκτικά μείγματα με τον αέρα. Το ειδικό βάρος του είναι 0,52 και 0,55.
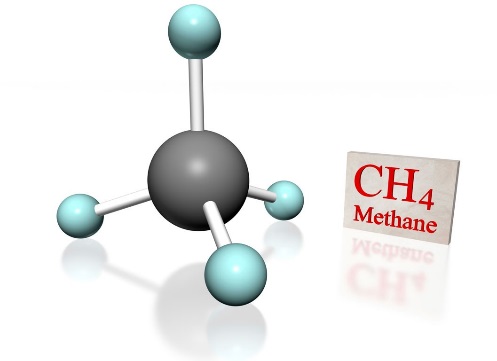
Το μεθάνιο είναι οργανική χημική ένωση, με χημικό τύπο CH4. Είναι άχρωμο και άοσμο και ανήκει στην κατηγορία των εύφλεκτων αερίων. Αποτελεί κύριο συστατικό του φυσικού αερίου (70 – 90%). Η σχετική αφθονία του στη Γη, η (σχετικά πάντα) μεγάλη ενεργειακή του απόδοση, η «καθαρή» καύση του και η χαμηλή του τιμή, το κάνουν πολύ ελκυστικό καύσιμο, ιδιαίτερα για παραγωγή ηλεκτρικής ενέργειας και οικιακή θέρμανση. Το μεθάνιο αντιδρά με οξυγόνο και καίγεται παράγοντας γαλαζωπή φλόγα υψηλής θερμοκρασίας. Είναι ελαφρύτερο από τον αέρα και έχει ειδικό βάρος ίσο με 0,59. Το L.E.L. είναι 4% κ.ο. και το U.E.L. είναι 14% κ.ο. στον αέρα. Είναι όμως εξαιρετικά εύφλεκτο και μπορεί να προκαλέσει έκρηξη σε μίγματα του με τον αέρα. Επίσης είναι δυνατό να προκαλέσει ασφυξία, γιατί απλά μπορεί να μειώσει τη συγκέντρωση του οξυγόνου σε κλειστούς χώρους. Επίσης είναι τοξικό για τον άνθρωπο όταν η συγκέντρωση του στον αέρα είναι πάνω από 10%.
Υδρογόνο (hydrogen, H2)

Το υδρογόνο μπορεί να παραχθεί με πολλούς διαφορετικούς τρόπους, αλλά οικονομικά η πιο σημαντική διεργασία περιλαμβάνει αφαίρεση υδρογόνου από υδρογονάνθρακες. Το βιομηχανικό υδρογόνο συνήθως παράγεται με αναμόρφωση με ατμό σε φυσικό αέριο. Σε υψηλές θερμοκρασίες (700 – 1000°C), ατμός αντιδρά με το μεθάνιο (CH4, κύριο συστατικό του φυσικού αερίου) και δίνει μονοξείδιο του άνθρακα (CO) και υδρογόνο. Μεγάλες ποσότητες υδρογόνου χρειάζονται στις πετροχημικές και χημικές βιομηχανίες. Η μεγαλύτερη (σε κατανάλωση) εφαρμογή του υδρογόνου είναι στην επεξεργασία (αναβάθμιση, upgrading) των ορυκτών καυσίμων. Οι κυριότεροι καταναλωτές υδρογόνου είναι στις πετροχημικές μονάδες που περιλαμβάνουν διεργασίες όπως υδρογονοαποθείωση.
Το υδρογόνο είναι πολύ εύφλεκτο και καίγεται στον αέρα σε ένα πολύ μεγάλο εύρος συγκεντρώσεων, από 4% – 75% κατ’ όγκο. (κατώτατο όριο 40000ppm και ανώτερο τα 750000ppm) Η θερμοκρασία αυτανάφλεξης του υδρογόνου στον αέρα είναι 500 0c. Η φλόγα που παράγεται από την καύση καθαρού υδρογόνου και καθαρού οξυγόνου εκπέμπει κυρίως υπεριώδες φως και γι’ αυτό είναι σχεδόν αόρατη από το ανθρώπινο μάτι. Επειδή το υδρογόνο είναι πολύ ελαφρύτερο από τον αέρα, οι φλόγες υδρογόνου τείνουν να ανυψωθούν τάχιστα και γι’ αυτό κάνουν μικρότερη ζημιά από τις φλόγες υδρογονανθράκων. Σε κλειστούς χώρους και σε μεγάλες συγκεντρώσεις υδρογόνου, υπάρχει κίνδυνος ασφυξίας για το προσωπικό. Γενικά το προϊόν αυτό δεν έχει τοξικολογικές επιδράσεις.
Υδρόθειο (hydrogen sulfide, H2S)
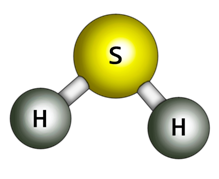
Το υδρόθειο χημική ένωση, που περιέχει υδρογόνο και θείο, με μοριακό τύπο H2S.
Ιδιαίτερα μεγάλες ποσότητες υδρόθειου λαμβάνονται κατά τη διαδικασία της αποθείωσης του πετρελαίου.
Είναι ιδιαίτερα τοξικό, βαρύτερο του αέρα (1,17 φορές) με τον οποίο μπορεί να δημιουργήσει εκρηκτικά μείγματα. Εύκολα αναφλέξιμο στις αντιδράσεις του με ισχυρά εξωθερμική αντίδραση. Έχει δυσάρεστη οσμή (σαν χαλασμένο αυγό), ενώ σε υψηλότερες συγκεντρώσεις έχει οσμή και γεύση γλυκίζουσα. Πολύ γρήγορα αναισθητοποιεί την όσφρηση. Έτσι η όσφρηση είναι ένας τρόπος ανιχνεύσεως του αερίου που δεν πρέπει να εμπιστευόμαστε. Το υδρόθειο είναι πολύ εκρηκτικό (4,3 μέχρι 46% ανά όγκο αέρα), καίγεται με γαλάζια φλόγα και το παράγωγο της καύσης του είναι το διοξείδιο του θείου (SO2) επίσης πολύ τοξικό αέριο.
Όταν ένα άτομο εισπνεύσει υδρόθειο, το αέριο δια μέσου του αναπνευστικού συστήματος περνάει στο αίμα. Ο οργανισμός αντιδρά και οξειδώνει (διασπά) το υδρόθειο, όσο πιο γρήγορα μπορεί, σε ακίνδυνες ενώσεις. Αν όμως, η ποσότητα είναι τόσο μεγάλη ώστε ο οργανισμός να μην μπορέσει να την εξουδετερώσει, το υδρόθειο συγκεντρώνεται στο αίμα και παραλύει μέσω του εγκεφάλου το νευρικό σύστημα που ελέγχει την αναπνοή. Οι πνεύμονες σταματούν και επέρχεται ασφυξία.
Βιβλιογραφία
Βικιπαίδεια
Βιβλιογραφία επικίνδυνων αερίων ΕΛ.ΠΕ.
Φωτογραφίες
Google photos
Ζαφειρίου Χ. Στέφανος
Πυροσβέστης διυλιστηρίων και πετροχημικών εγκαταστάσεων.
Διαχειριστής εκτάκτων αναγκών.
SSI Dive Master pro – Διασώστης Δυτών.
Εθ. Αρχιπυροσβέστης Π.Σ.







